


新闻资讯
Adv Mater |多肽纤维抑制内皮细胞介导的T淋巴细胞凋亡提高三阴性乳腺癌化疗免疫治疗效果
2023-10-25 15:12
肿瘤内皮屏障和缺乏CD8+ T细胞浸润是阻碍三阴性乳腺癌(TNBC)治疗的两大障碍。其中,肿瘤相关内皮细胞(TECs)免疫调节分子的异常表达诱导免疫逃逸,研究表明,TECs通过上调Fas配体(FasL)的表达,诱导浸润性T淋巴细胞凋亡,严重限制了T细胞的肿瘤浸润。因此,调控TECs的FasL表达联合诱导肿瘤细胞的免疫原性细胞死亡(ICD)是潜在的肿瘤化疗免疫治疗新策略。
2023年10月17日,烟台新药创制山东省实验室/上海药物研究所李亚平团队与上海科技大学张鹏程团队在Advanced Materials上发表了“Inhibiting endothelial cell-mediated T lymphocyte apoptosis with integrin-targeting peptide-drug conjugate filaments for chemoimmunotherapy of triple-negative breast cancer”的研究论文,构建了基于多肽-药物偶联物(PDC)自组装形成的多肽纳米纤维,协同调控血管内皮屏障,联合ICD诱导的肿瘤免疫治疗提高TNBC的治疗效果。
研究人员分别将7-乙基-10-羟基喜树碱(SN38)连接到RGDR或HKD多肽,构建了谷胱甘肽响应的PDC药物,在水溶液中能够自组装成纳米纤维,并且进一步筛选SN38-RGDR与SN38-HKD的比例,制备了同时靶向肿瘤细胞和TECs的纳米纤维SN38-HKD/RGDR。
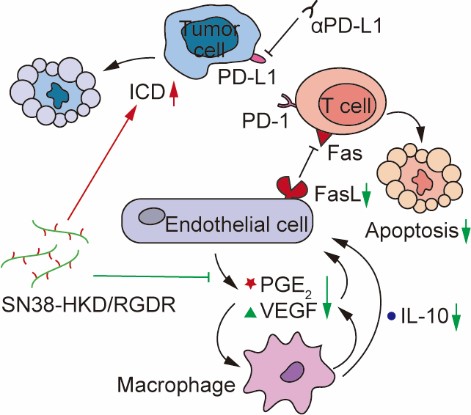
SN38-HKD/RGDR作用机理
研究发现,SN38-HKD/RGDR能够诱导肿瘤细胞的免疫原性细胞死亡,同时降低前列腺素E2(PGE2)、骨髓来源巨噬细胞和肿瘤细胞的血管内皮生长因子(VEGF)和白介素10(IL-10),协同下调TECs的FasL表达,增强CD8+ T细胞的浸润和存活,从而抑制原发肿瘤的生长和肺转移。
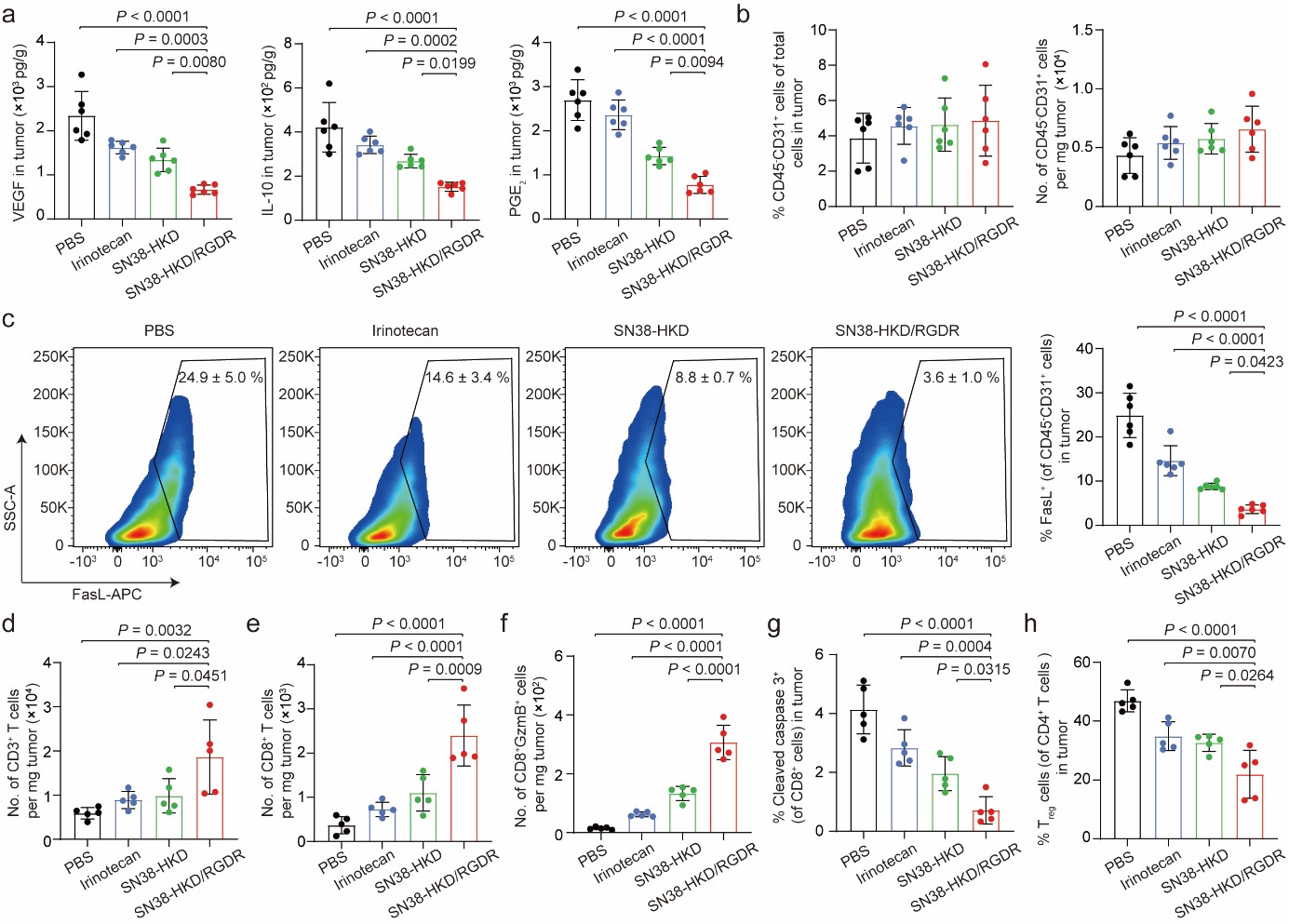
SN38-HKD/RGDR协同增强抗肿瘤免疫
烟台新药创制山东省实验室李亚平研究员和上海科技大学张鹏程研究员为本文的共同通讯作者,上海药物研究所博士研究生蔡颖和硕士研究生朱彬毓为本文共同第一作者。该研究得到了国家重点研发计划、国家自然科学基金、中国科学院等项目的资助。
全文链接
https://doi.org/10.1002/adma.202306676
(供稿部门:李亚平课题组;供稿人:曹海强)
Adv Mater |多肽纤维抑制内皮细胞介导的T淋巴细胞凋亡提高三阴性乳腺癌化疗免疫治疗效果
2023-10-25 15:12
肿瘤内皮屏障和缺乏CD8+ T细胞浸润是阻碍三阴性乳腺癌(TNBC)治疗的两大障碍。其中,肿瘤相关内皮细胞(TECs)免疫调节分子的异常表达诱导免疫逃逸,研究表明,TECs通过上调Fas配体(FasL)的表达,诱导浸润性T淋巴细胞凋亡,严重限制了T细胞的肿瘤浸润。因此,调控TECs的FasL表达联合诱导肿瘤细胞的免疫原性细胞死亡(ICD)是潜在的肿瘤化疗免疫治疗新策略。
2023年10月17日,烟台新药创制山东省实验室/上海药物研究所李亚平团队与上海科技大学张鹏程团队在Advanced Materials上发表了“Inhibiting endothelial cell-mediated T lymphocyte apoptosis with integrin-targeting peptide-drug conjugate filaments for chemoimmunotherapy of triple-negative breast cancer”的研究论文,构建了基于多肽-药物偶联物(PDC)自组装形成的多肽纳米纤维,协同调控血管内皮屏障,联合ICD诱导的肿瘤免疫治疗提高TNBC的治疗效果。

研究人员分别将7-乙基-10-羟基喜树碱(SN38)连接到RGDR或HKD多肽,构建了谷胱甘肽响应的PDC药物,在水溶液中能够自组装成纳米纤维,并且进一步筛选SN38-RGDR与SN38-HKD的比例,制备了同时靶向肿瘤细胞和TECs的纳米纤维SN38-HKD/RGDR。

SN38-HKD/RGDR作用机理
研究发现,SN38-HKD/RGDR能够诱导肿瘤细胞的免疫原性细胞死亡,同时降低前列腺素E2(PGE2)、骨髓来源巨噬细胞和肿瘤细胞的血管内皮生长因子(VEGF)和白介素10(IL-10),协同下调TECs的FasL表达,增强CD8+ T细胞的浸润和存活,从而抑制原发肿瘤的生长和肺转移。

SN38-HKD/RGDR协同增强抗肿瘤免疫
烟台新药创制山东省实验室李亚平研究员和上海科技大学张鹏程研究员为本文的共同通讯作者,上海药物研究所博士研究生蔡颖和硕士研究生朱彬毓为本文共同第一作者。该研究得到了国家重点研发计划、国家自然科学基金、中国科学院等项目的资助。
全文链接
https://doi.org/10.1002/adma.202306676
(供稿部门:李亚平课题组;供稿人:曹海强)